Question
Énoncé
Déterminer l'enthalpie molaire standard de formation de H2O (l) à 373 K en kJ.mol-1.
Données :
\(\Delta_fH°(H_2O, l ; 298 K)\) = - 285,2 kJ.mol-1.
CP (H2O, l) = 75,47 J.mol-1.K-1 entre 273 K et 373 K.
CP (H2, g) = 27,29 + 3,26 10-3 T + 0,5 105 T-2 (J.mol-1.K-1) entre 298 K et 3000 K.
CP (O2, g) = 29,97 + 4,18 10-3 T - 1,67 105 T-2 (J.mol-1.K-1) entre 298 K et 3000 K.
Aide simple :
La connaissance de :
l'enthalpie molaire de réaction à une température T ;
des fonctions décrivant comment varient avec la température T les capacités calorifiques molaires à pression constante des réactifs et produits
suffisent, en l'absence de changements d'état des réactifs et/ou des produits, pour déterminer l'enthalpie molaire de réaction à une température T' \(\neq\) T.
Rappel de cours :
A partir des équations de réactions et des changements d'état, on peut établir un diagramme de Hess ou une combinaison de transformations qui permettent d'obtenir les relations qui mènent à la solution.
Résultat
Correction
Explications
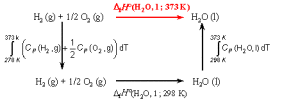
Diagramme de Hess :
D'où la formule et l'application numérique suivantes :
\(\Delta_f H°(H_2O, l ; 373K) =\Delta_f H°(H_2O, l ; 298K) +\displaystyle \int_{298 K}^{373 K} \left(Cp_{H_2O, l} - Cp_{H_2, g} - \frac{1}{2}Cp_{O_2, g} \right)dT\)
\(Cp_{H_2O, l} - Cp_{H_2, g} - \frac{1}{2}Cp_{O_2, g} = 75,47 - 27,29 - 0,00326T - 0,5.10^5 \frac{1}{T^2} - \frac{1}{2} \left( 29,97 + 0,00418T - 1,67.10^5 \frac{1}{T^2}\right)\)
\(\Delta_f H°(H_2O, l ; 373K) = -285200 + \displaystyle \int_{298 K}^{373 K} \left(33,195 - 0,00535T + 0,335.10^5 \frac{1}{T^2} \right)dT\)
\(= -285200 + \bigg[ 33,195T - 0,00535 \frac{T^2}{2} - 0,335.10^5 \frac{1}{T} \bigg]_{298 K}^{373 K}\)
\(=- 285200 + 33,195 (373 - 298)\frac{0,00535}{2} (373² - 298²) - 0,335.10^5 (\frac{1}{373} - \frac{1}{298})\)
\(\Delta_f H°(H_2O, l ; 373K)\) = - 282789 J.mol-1 = -282,8 kJ.mol-1