Introduction
Comme leur nom l'indique, les éléments \(p\), qui constituent les colonnes 13 à 18 du tableau périodique, correspondent au remplissage de la sous-couche \(p\) (\(l = 1\) et \(m= -1 ;0 ;1\)). La configuration électronique de leur couche de valence est donc , avec \(n\), le nombre quantique principal, variant de 2 à 6, et \(x\), le nombre d'électrons occupant la sous-couche \(p\), pouvant varier de 1 (éléments de la colonne 13) à 6 (éléments de la colonne 18). Ces différents éléments sont rassemblés au tableau ci-dessous .
Présentation des éléments p dans la classification périodique.
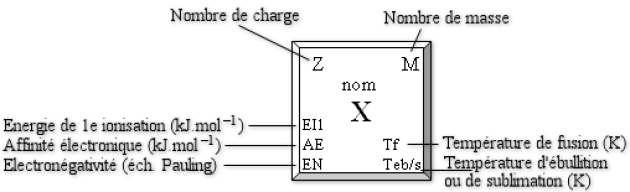
Propriétés atomiques \((\mathrm{EI_i,~r_A ,~AE ,~EN} )\) et températures de changement d'état
On note que beaucoup parmi ces éléments nous sont familiers à un titre ou un autre. On y trouve tous les non-métaux et semi-conducteurs, ainsi que quelques métaux. Mis à part l'hydrogène, tous les éléments de base de la chimie organique (\(\textrm C\), \(\textrm N\), \(\textrm O\)) sont présents.
Certains éléments sont connus depuis des siècles, comme \(\textrm{Sn}\), \(\textrm{Pb}\), \(\textrm{As}\), \(\textrm S\), \(\textrm{Cl}\), \(\textrm{Br}\),\( \textrm I\), \(\textrm P\), \(\textrm N\), \(\textrm O\), \(\textrm C\) (cela se retrouve dans leur nom qui ne finit pas en « -ium »). On considèrera à part la famille des gaz rares (colonne 18), formée d'éléments n'ayant pratiquement aucune réactivité chimique du fait de leur couche de valence saturée \(ns^2np^6\).
Ces éléments présentent une grande diversité de propriétés tant physiques que chimiques. Nous allons essayer de l'expliquer dans la suite, en se basant sur les propriétés fondamentales des atomes.
A la suite de cette introduction, nous développerons plus particulièrement les propriétés de quelques-uns de ces éléments du fait de leur importance, à savoir l'azote, l'oxygène, et le chlore.
