Propriétés physiques et microscopiques
Propriétés physiques
Le chlore se présente à température ambiante sous forme de gaz de couleur jaune-vert. Il est assez peu soluble dans l'eau (environ \(5\textrm{ g.L}^{-1}\) à la température ambiante).
Sa densité est 2,49 et les températures de changement d'état sont pour la fusion \(T_{\textrm{fusion}}=-101 °\textrm C\) et pour l'ébullition \(T_{\textrm{eb}}=-35 °\textrm C\).
Structure et propriétés microscopiques
Schéma de Lewis

Diagramme d'OM-CLOA
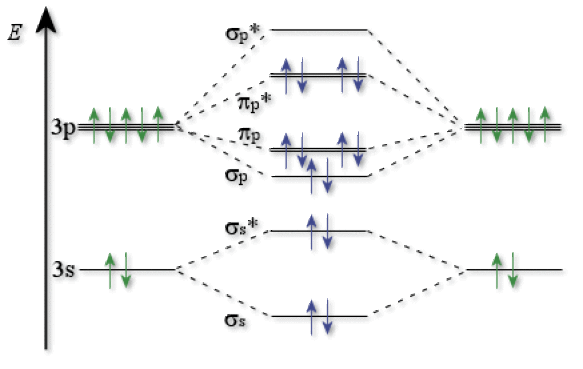
On tire de ce diagramme plusieurs propriétés :
La liaison est simple (l'indice de liaison \(\textrm{i.l.}=1\)). On a donc une longueur de liaison assez importante (\(2\AA\)) et une relative fragilité de la molécule (elle peut être décomposée par absorption d'un photon UV, par exemple).
\(\textrm{Cl}_2\) est diamagnétique (tous les électrons sont appariés).
La couleur jaune-vert provient de transitions d'électrons \(\pi^*_\textrm p\) vers le niveau \(\sigma^*_\textrm p\), dont l'absorption se situe dans le rouge et le bleu.
Rappel : Indice de liaison
On rappelle que l'indice de liaison (\(\textrm{i.l.}\)) vaut : \(\textrm{i.l.}=\frac{1}{2}(\textrm{nbre d'électrons liants} - \textrm{nbre d'électron antiliants})\), soit ici \(\textrm{i.l.}=\frac{1}{2}((2+2+4)-(2+4))=1\).