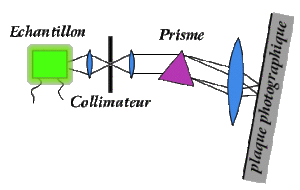
Spectres d'émission des atomes
Quand on chauffe des sels de certains métaux alcalins ou alcalino-terreux, ou quand on provoque une décharge électrique dans un gaz, on constate l'émission de lumière à certaines longueurs d'ondes bien précises, caractéristiques des éléments.
Les sels de sodium chauffés produisent une lumière jaune alors que les sels de potassium émettent dans le violet et les sels de baryum dans le vert clair.
Une décharge électrique dans un gaz de néon produit une lumière rouge orangée alors que la vapeur de mercure émet une lumière bleue-verte. L'hydrogène excité électriquement produit un rayonnement entre le bleu et le violet.
On obtient alors ce que l'on appelle des spectres de raies fines qui montrent que l'émission se produit pour des longueurs d'ondes particulières. Ainsi, Kirchhoff et Bunsen ont déterminé dès 1861 que le sodium produit une paire de raies d'émission très proches (le doublet du sodium) à 589 nm et 589,6 nm.
La compréhension même de ce phénomène échappait à l'analyse dans le cadre des théories connues au début du vingtième siècle. L'émission atomique était en contradiction avec l'enseignement de la physique classique qui ne pouvait prévoir qu'une émission continue autodestructrice.