Le modèle de Bohr
En 1913, Niels Bohr publia un article intitulé "De la constitution des atomes et des molécules" dans lequel il tentait de concilier un modèle atomique planétaire pour l'atome d'hydrogène et la quantification observée sur son spectre d'émission.

Niels Bohr
Son hypothèse de base reposait sur les postulats suivants :
L'électron circule à vitesse et énergie constante sur des orbites circulaires particulières sur lesquelles il y a exacte compensation entre l'attraction coulombienne du noyau et la force centrifuge.
Ces orbites particulières se limitent à celles pour lesquelles l'action, produit de la quantité de mouvement et de la longueur de l'orbite, est un multiple de la constante de Planck.
Le changement d'orbite se produit par absorption ou émission d'un photon. L'énergie du photon absorbé ou émis correspond à la différence d'énergie des deux orbites.
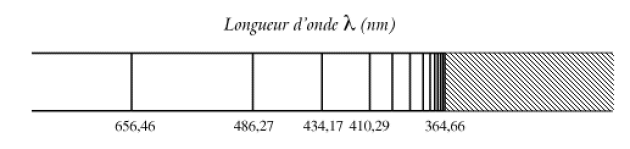
Le modèle de Bohr de l'atome d'hydrogène est un modèle construit avant tout pour rendre compte de l'existence des spectres de raies atomiques. Il conjugue le modèle planétaire classique de Rutherford et une condition de quantification des orbites permises. Son mérite principal tient à sa capacité à reproduire théoriquement les spectres de raies observés.