Le mélange s-p-p-p
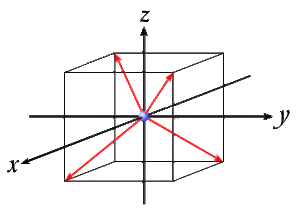
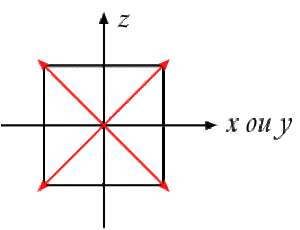
Dans la molécule tétraédrique \(\textrm{CH}_4\), la polarisation du carbone par les quatre atomes d'hydrogène conduit à l'introduction de quatre orbitales hybrides appelées hybrides \(\textrm{sp}^3\). Ces trois hybrides sont simulées par des combinaisons linéaires normées de l'orbitale \(2\textrm s\) et des trois orbitales \(2\textrm p\). Elles remplacent les 4 orbitales de valence \(2\textrm s\) et \(2\textrm p\).
Ce type d'hybridation se rencontre pour les atomes de type \(\textrm{AX}_4\), \(\textrm{AX}_3\textrm E\) et \(\textrm{AX}_2\textrm E_2\) et \(\textrm{AXE}_3\).
On combine d'abord les orbitales \(2\textrm p_x\) et \(2\textrm p_y\) avec des angles de mélange de 45, 135, 225 et 315 degrés pour orienter convenablement les projections dans le plan \(x\textrm Oy\).
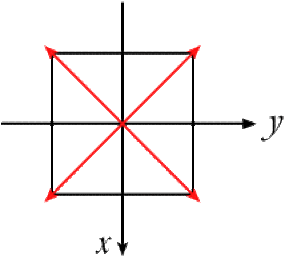
Il reste alors à combiner chacune des orbitales \(2\textrm p\) correctement orientée avec l'orbitale \(2\textrm s\).