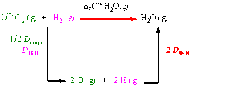Question 1
Énoncé
Déterminer la valeur moyenne de l'énergie de dissociation, en kJ.mol-1, de la liaison O-H dans la molécule d'eau.
Données pour 25°C :
Énergie de dissociation de la liaison H-H : DH-H = 432 kJ.mol–1.
Énergie de dissociation de la liaison O=O : DO=O = 493,6 kJ.mol–1.
Énergie interne standard de formation de H2O gaz : \(\Delta_fU°(H_2O, g)\) = - 240,6 kJ.mol–1.
Aide simple :
L'énergie de la liaison X-Y (DX-Y) est l'énergie interne \(\Delta_rU\) de la réaction : X-Y (g) = X (g) + Y (g).
Rappel de cours :
Deux méthodes équivalentes peuvent être utilisées, exploitant le fait que l'énergie interne est une fonction d'état :
construction d'un cycle de Hess
ou combinaison linéaire d'équations de réaction.
Résultat
Correction
Explications
Méthode utilisant un cycle de Hess :
Comme U est une fonction d'état, il vient : \(\Delta_fU°(H_2O, g) = \frac{1}{2} D_{O=O} + D_{H-H} - 2 D_{O-H}\)
d'où : \(D_{O-H} = \frac{1}{2} [\frac{1}{2} D_{O=O} + D_{H-H} - \Delta_fU°(H_2O, g)] = \frac{1}{2} [(\frac{1}{2} \times 493,6) + 432 - (- 240,6)]\) = 459,7 kJ.mol-1.
Les tables donnent DO-H = (458,8 ± 1,4) kJ.mol-1.
Méthode utilisant une combinaison linéaire d'équations de réactions :
\(\frac{\begin{array}{c c c c c c } &&\frac{1}{2} O_2 (g)&=& O(g)&1/2D_{O=O} \\ &&H_2(g)&=& 2 H (g)& D_{H-H} \\ O(g)&+&2H(g)&=&H_2O(g)& -2D_{O-H} \end{array}}{\begin{array}{c c c c c c} \frac{1}{2} O_2(g)&+&H_2 (g)&=&H_2O (g) & \Delta_fU°(H_2O, g) \\ \end{array}}\)
En additionnant les énergies de liaison mises en jeu par ces transformations, on retrouve, après réarrangemnt, l'énergie de la liaison O-H.