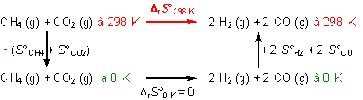Question 1
La réaction de reformage du méthane CH4 par le dioxyde de carbone CO2 s'écrit :
CH4 (g) + CO2 (g) \(\rightarrow\) 2 H2 (g) + 2 CO (g) (1)
Déterminer la valeur de l'entropie standard de réaction \(\Delta_rS°\) de (1) à 298 K et réfléchir aux raisons qui permettent de dire pourquoi cette valeur doit être positive. La réponse sera donnée en J.mol-1.K-1.
Données :
Entropies absolues standard S°298K (en J.mol-1.K-1) | |
|---|---|
CH4 (g) | 186,2 |
CO2 (g) | 213,6 |
CO (g) | 197,6 |
H2 (g) | 130,6 |
Aide simple :
L'entropie de réaction est reliée à l'état de désordre : elle est positive lorsque l'état de désordre augmente, ce qui est le cas pour cette réaction puisque \(\sum \nu_{i,gaz}\) > 0.
Rappel de cours :
On peut imaginer le cycle suivant :
Rappel : l'entropie est une fonction d'état lorsque l'on suit un chemin réversible.
On retrouve ainsi les entropies absolues des réactifs et des produits (flèches verticales) et les entropies standard de réaction.
A 0 K, les entropies standard sont nulles.