Les symétries des orbitales
Comme dans les atomes, les orbitales servant à bâtir la structure électronique des molécules doivent respecter certaines règles de symétrie. Ces règles sont dictées par la symétrie du champ d'attraction par les noyaux de la molécule. Dans l'ion \(\textrm H_2^+\) ou la molécule \(\textrm H_2\) par exemple, on distingue l'axe de la liaison qui constitue un axe de révolution. On considère aussi que les deux atomes s'échangent par un centre de symétrie.
Sur la figure ci-contre, on a représenté les deux noyaux de \(\textrm H_2\) en rouge. L'axe doré est l'axe de révolution. L'origine des axes est sur le centre de symétrie.
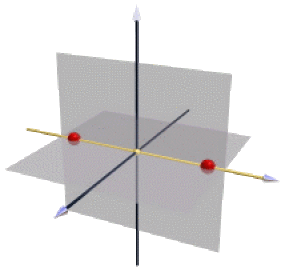
Les orbitales moléculaires que l'on étudiera dans ce chapitre sont de symétrie de révolution, invariantes par une rotation quelconque autour de l'axe de la liaison.
Ces OM sont dites de symétrie \(\sigma\).

On distingue alors les orbitales moléculaires symétriques par rapport au centre de symétrie.
Ces OM sont dites de symétrie \(g\) (gerade en allemand).
On note le symbole de symétrie \(\sigma_g\).
Dans l'orbitale symétrique figurée ci-contre, tout point de l'espace et son symétrique donnent la même valeur de l'orbitale.
Le second type d'orbitales moléculaires est antisymétrique par rapport au centre de symétrie.
Ces OM sont dites de symétrie \(u\) (ungerade en allemand).
On note le symbole de symétrie \(\sigma_u\).
Sur la figure ci-contre, on a figuré l'antisymétrie et donc le changement du signe de l'OM par rapport au centre de symétrie en utilisant deux couleurs.

Ces étiquettes de symétrie sont le pendant moléculaire de celles utilisées pour les atomes (orbitales \(\textrm s\), \(\textrm p\), \(\textrm d\), \(\textrm f\), ...)