Structure du laiton
Durée : 10 mn
Note maximale : 4
Question
Le laiton est un alliage cuivre-zinc qui dérive de la structure cfc du cuivre. Des atomes de zinc remplacent certains atomes de cuivre.
Quelle est la formule de l'alliage lorsque 4 atomes de zinc occupent les sommets de la maille ?
Quel est le pourcentage pondéral de Zn dans l'alliage ?
On donne :
\(\qquad\) \(\textrm{M}_{\textrm{Cu}} = \mathrm{63,55}~\textrm{g.mol}^{-1}\)
\(\qquad\) \(\textrm{M}_{\textrm{Zn}} = \mathrm{65,39}~\textrm{g.mol}^{-1}\)
Solution
1. Pour visualiser les positions des atomes, on a représenté la maille ci-dessous avec le calcul du nombre d'atomes de cuivre et de zinc.
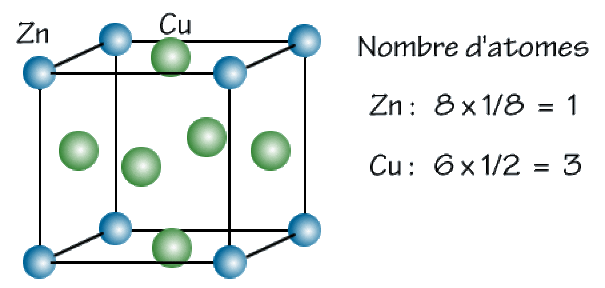
La formule est\(\textrm{Cu}_{3}\textrm{Zn}\).
2. Pour calculer le pourcentage pondéral de zinc, on calcule d'abord la masse molaire du groupement formulaire :\(\qquad\) \(M = \mathrm{63,55}\times3 + \mathrm{65,39} = \mathrm{256,04}~\textrm{g.mol}^{-1}\)
Il n'y a qu'un atome de zinc dans le groupement :\(\qquad\) \(\%\textrm{Zn} = \frac{\mathrm{65,39}}{\mathrm{256,04}}\times100 = \mathrm{25,54}\%\)