Les orbitales de valence
Les trois hybrides coplanaires s'obtiennent en utilisant 3 angles de mélange p + p distincts, qui correspondent aux trois directions caractéristiques de la figure de répulsion.

Dans la molécule \(\textrm{BH}_3\), les trois hybrides sont équivalentes par symétrie et pointent chacune vers un des hydrogènes à 120° l'un de l'autre. On prend alors comme configuration électronique du béryllium hybridé :
\(\mathbf{1\textrm s^2(\textrm{sp}^2)^3}\)
On a représenté ci-contre les trois hybrides coplanaires.
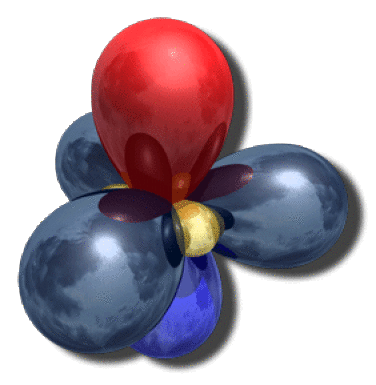
Sur la figure ci-contre, on a représenté en perspective les quatre orbitales de valence du bore :
les trois hybrides \(\textrm{sp}^2\) (reflets métalliques)
l'orbitales \(2\textrm p_z\) (en bleu et rouge) orthogonale aux hybrides et vide dans \(\textrm{BH}_3\).
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.