Couplages
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Par abus de langage, on dit souvent "le couplage ne passe pas à travers les hétéroatomes". En fait ceci est réducteur et même faux dans certaines conditions.
Examinons le cas du propanol \(\textrm{CH}_3\textrm{-CH}_2\textrm{-CH}_2\textrm{-OH}\).
Le proton alcoolique n'est pas couplé alors qu'il existe deux hydrogènes en position béta : \(\textrm{H-O-CH}_2\textrm-\) et \(\textrm{H-C-CH}_2\textrm-\). En remplaçant l'oxygène \(\textrm O\) par un carbone \(\textrm C\), nous savons qu'un couplage \(\textrm{}^3J\) serait observé. Que se passe-t-il donc pour que le couplage à travers l'oxygène ne soit pas observé ? C'est ce que nous allons voir maintenant...
L'électronégativité de l'oxygène est supérieure à celle de l'hydrogène... Dans l'échelle de Pauling, pour \(\textrm H\) : 2,3 et pour \(\textrm O\) : 3,8. Du fait de cette électronégativité, la liaison \(\textrm{OH}\) est polarisée, l'hydrogène présente un caractère mobile non négligeable et des liaisons hydrogènes intermoléculaires vont s'établir.
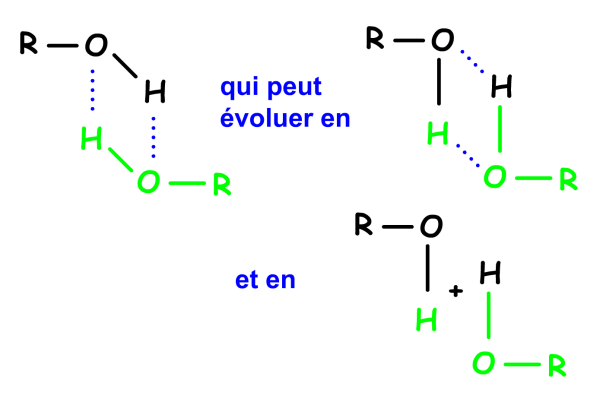
On observe des échanges intermoléculaires. Cette mobilité est associée aux hétéroatomes, particulièrement à l'oxygène et à l'azote qui donnent des liaisons \(\textrm{O-H}\) et \(\textrm{N-H}\) polarisées.
Ainsi, sans condition particulière, les hydrogènes alcooliques s'échangent rapidement et donc n'ont pas une durée de vie suffisante en position de proximité des hydrogènes portés par le carbone en béta \(\textrm{-CH}_2\textrm{-O-R}\) pour percevoir leurs états de spin et donc être couplés. On observe donc un singulet comme signal résultant, assez souvent large.
Cet hydrogène mobile voit des environnements divers et de ce fait, le domaine des champs qui induisent sa résonance est plus important ce qui explique la largeur du signal observé pour les protons alcooliques. Pour des raisons similaires, un signal large sera souvent observé pour les protons attachés à l'azote >N-H.
Cette mobilité peut être accélérée avec l'adjonction d'une trace d'acide, alors que la présence d'un solvant très basique va stabiliser l'hydrogène grâce à une liaison hydrogène plus forte.
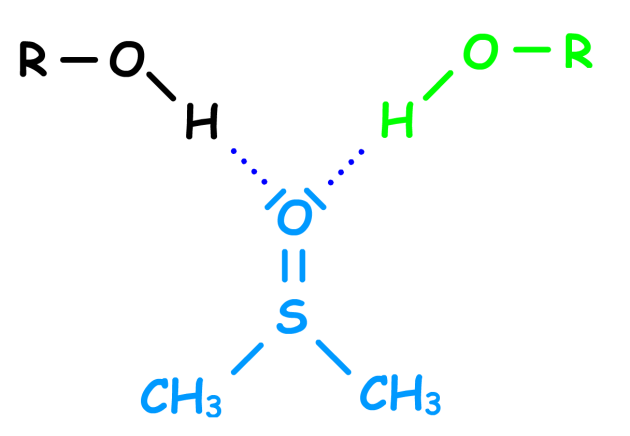
C'est ce qui se passe quand on ajoute du Diméthyle sulfoxyde DMSO \(\textrm{(CH3)}_2\textrm{S=O}\). Cet ajout bloque les échanges protoniques et dans ces conditions, il devient possible de voir le couplage du proton alcoolique. Voyons cela en détails...
Dès que l'on ajoute du diméthyle sulfoxyde \(\textrm{(CH3)}_2\textrm{S=O}\) (DMSO) à un alcool, il se crée des liaisons hydrogènes avec l'oxygène du DMSO. Cela a pour effet d'entraver la mobilité de l'hydrogène alcoolique et provoque l'observation du couplage à travers l'hétéroatome. Ceci est un moyen de déterminer la classe d'un alcool...
On observera
un triplet pour le \(\textrm{OH}\) d'un alcool primaire, \(\textrm{-CH2-OH}\),
un doublet pour le \(\textrm{OH}\) d'un alcool secondaire,>\(\textrm{CH-OH}\),
un singulet pour le \(\textrm{OH}\) d'un alcool tertiaire, \(\textrm{C-OH}\).
Bien entendu, la multiplicité du signal du \(\textrm{-CH}_2\textrm-\) ou du \(\textrm{>CH-}\) porteur du \(\textrm{OH}\) sera également augmentée par ce couplage... Le \(\textrm{}3J\) à travers l'oxygène a une valeur de l'ordre de 5 hertz.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Cas A : Le spectre de l'éthanol à 95° donc non pur... donne un signal "patatoïdique" pour le OH. Du fait de la mobilité du H, on n'observe pas de couplage à travers l'hétéroatome.
Cas B : Le spectre de l'alcool pur fait apparaître un couplage à travers l'oxygène égal à 5 Hz alors que le couplage vicinal est de 7 Hz. On observe un triplet (OH) et un quadruplet dédoublé (CH2).
Cas C : Avec une trace d'acide ajoutée à l'échantillon, on augmente la mobilité du OH, son signal devient plus fin, son déplacement chimique plus fort et on n'a toujours pas de couplage.
Cas D : Avec du diméthylsulfoxyde deutéré, on bloque le OH et on force le couplage...Notez le signal orange (quintuplet), c'est celui de la trace de DMSO non deutéré CD3(SO)CHD2. Vous trouverez l'explication de l'existence et de la multiplicité de ce signal dans le dernier sous-chapitre des hétéroatomes (noyaux à spins supérieur à 1/2).