Thiols
Les composés soufrés
Les autres fonctions sont parfois décrites comme dérivant des homologues plus légers dans la même colonne du tableau de Mendeleïev, les dérivés soufrés renvoient au dérivés oxygénés , les dérivés sylilés aux hydrocarbures, ...
La présence d'un soufre peut passer inaperçue si l'on ne travaille que sur le pic parent P ; en effet, la masse de l'isotope le plus léger et le plus abondant est 32u que l'on peut confondre avec 2 fois 16, pour 2 oxygènes. Pour éviter cette erreur (assez souvent rencontrée), il suffit d'analyser l'ensemble des pics parents, ce qui est d'ailleurs conseillé dans tous les cas et avant toute analyse des fragments.
Le \(\textrm{}^{32}\textrm S\) est accompagné par deux isotopes \(\textrm{}^{33}\textrm S\) et \(\textrm{}^{34}\textrm S\), ce dernier ayant une intensité relative inattendue pour un P + 2 de 4.4%. Ainsi, un P + 2 d'intensité observable de l'ordre de 4 à 5 % (du P) est un bon détecteur de soufre \(\textrm S\) et cela reste vrai pour tous les fragments qui contienne ce soufre \(\textrm S\). Pour \(2\textrm S\), l'intensité relative du P + 2 est de 2 fois 4.4% et pour n \(\textrm S\) de n fois 4.4% (en l'absence de \(\textrm{Cl}\) ou \(\textrm{Br}\) qui perturbent l'intensité du P + 2).
Thiols ou mercaptans
Pour les \(\textrm{RSH}\), on peut établir un parallèle avec les alcools.
Le pic parent est souvent plus présent et on observe des P - \(\textrm{SH}\), soit P - 33 et aussi des P - 34, soit la perte de \(\textrm H_2\textrm S\) équivalente à la perte de \(\textrm H_2\textrm O\) pour les alcools. Ces pertes interdisent bien souvent l'observation des fragments soufrés ou en réduisent fortement l'intensité. Ces fragments (saturés) soufrés sont très caractéristiques car ils de différencient des masses des fragments alkyles par 4u soit 33 (\textrm{SH}), 47 (\(\textrm{CH}_2\textrm{SH}\)), 61 (\(\textrm C_2\textrm H_4\textrm{SH}\)), 75 (\(\textrm C_3\textrm H_6\textrm{SH}\)),.....
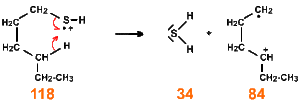
Pour le 1-hexanethiol, le pic parent à 118 ( 30 %) est accompagné d'un P + 2 (2 %) ce qui est caractéristique des produits soufrés.
Les fragment essentiels sont ceux issus de la chaîne alkyle (27 / 29, 41 / 43, 57 pic de base, 69) ; on observe néanmoins des ions soufrés à 47 (coupure \(\beta\)), 61.
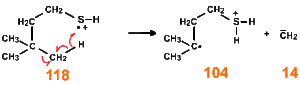
Pour le 3,3-diméthyle, 1-butanethiol, la situation est assez similaire.
Le pic parent est moins intense du fait de la ramification de la chaîne alkyle mais on observe encore (bien que faible) un P + 2 dû au \(\textrm{}^{34}\textrm S\). L'ion 104 est assez particulier puisqu'il figure un P - 14 en lieu et place du P - 15 que laissait prévoir le carbone triméthylé de bout de chaîne ; cet ion est issu du réarrangement signalé précédemment (retour d'un H sur le soufre à l'origine du P - \(\textrm H_2\textrm S\)), mais la concurrence du carbocation tertiaire est la plus forte et on observe le P - 14.
L'ion 85 est donc un P - 33, soit P - \(\textrm{SH}\), supérieur (à cause du P - 14) au 84 encore observable. Les fragments essentiels sont encore ceux issus de la chaîne alkyle (27 / 29, 39 / 41 / 43 pic de base, 55 / 57, 69 / 71) ; on observe néanmoins des ions soufrés à 47 (coupure \(\beta\)), 61, 75 et, très faible, une série allant de 32 à 35 sur laquelle nous reviendrons.