Schémas de résonance (2)
Durée : 8 mn
Note maximale : 4
Question
Etablir les schémas de Lewis résonants de l'ozone\(\textrm{O}_{3}\)et de la molécule\(\textrm{SO}_{2}\).
Solution
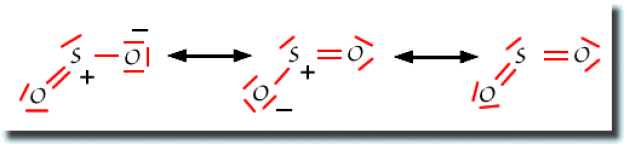
Les schémas de Lewis sont indiqués sur la figure ci-dessous.
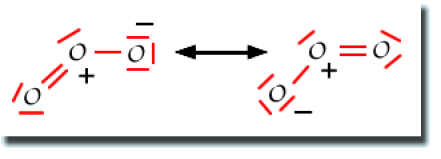
Dans le cas de l'ozone, il n'y a que deux formules résonantes symétriques dans lesquelles les oxygènes obéissent à la règle de l'octet. Elles mettent en évidence l'apparition de liaisons polarisées O-O.
Dans le cas de la molécule\(\textrm{SO}_{2}\), le soufre central peut accommoder plus de huit électrons en utilisant des orbitales de type d. Il y a donc dans le schéma de résonance une structure de Lewis sans charges partielles. Le poids de cette structure neutre est non négligeable.