Energie potentielle moléculaire
Pour l'ion moléculaire dans son état fondamental, l'électron est porté par l'orbitale moléculaire \(\sigma_g\). On rajoute la répulsion internucléaire à l'énergie électronique pour obtenir l'énergie potentielle moléculaire de l'état fondamental \(\sigma_g\).
On fait de même pour l'état excité \(\sigma_u\).
On obtient les courbes \(V(R_\textrm{AB})\) représentées ci-dessous pour ces deux états. Le zéro de l'énergie correspond à l'énergie d'un atome d'hydrogène et d'un proton séparés (\(E_\textrm H\)).
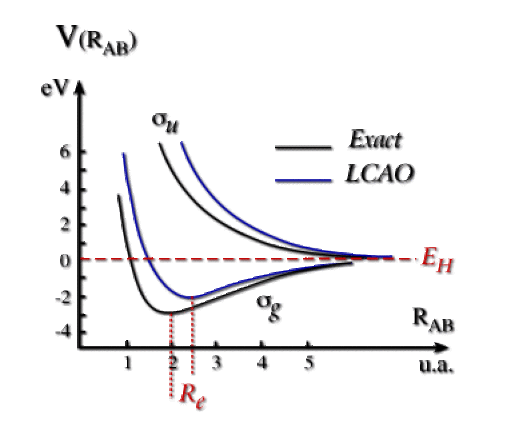
On a aussi représenté les courbes exactes (le problème de \(\textrm H_2^+\) est soluble analytiquement mais extrêmement compliqué mathématiquement). L'état fondamental présente un puits d'énergie potentielle : la stabilisation de l'énergie électronique par rapport à l'énergie des deux atomes est suffisante pour contrebalancer la répulsion entre les deux noyaux et assurer la stabilité de la liaison chimique.
L'état excité \(\sigma_u\) ne présente pas de puits d'énergie potentielle : il est dissociatif.