Potentiels de couples redox dépendants
Lorsqu'un élément peut apparaître avec plusieurs degrés d'oxydation, on peut déterminer le potentiel standard d'un couple connaissant ceux d'autres couples du même élément.
Exemple :
Pour l'or, on a \(E^0_1 (\textrm{Au}^+ / \textrm{Au}) = \textrm{1,68 V}\) et \(E^0_2 (\textrm{Au}^{3+} / \textrm{Au}) = \textrm{1,50 V}\). Déterminons le potentiel standard \(E^0_3\) du couple \(\textrm{Au}^{3+} / \textrm{Au}\) .
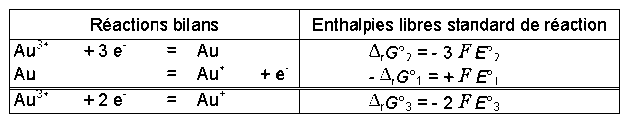
Sachant que \(\Delta_rG° = -n.F.E°\) pour un couple écrit dans le sens de la réduction, on va utiliser les propriétés de fonction d'état de la fonction enthalpie libre \(G\). On combine les 2 premières réactions de couple pour obtenir la troisième.
Soit
\(-2.F.E^0_3 = -3.F.E^0_2 + F.E^0_1\)
d'où
\(E^0_3 = \frac{3.E^0_2 - E^0_1}{2}\)
A.N. : \(E^0_3=\textrm{1,41 V}\)