Introduction
La spectroscopie Infra Rouge permet l'étude des vibrations moléculaires. Parmi celles-ci les vibrations d'élongation sont particulièrement intéressantes en IR. C'est pourquoi l'ensemble de ce chapitre leur est consacré. Les autres vibrations, dites de déformations seront introduites lors de l'étude des fonctions dans le prochain paragraphe.
Nous étudierons successivement les élongations des liaisons associant un atome d'hydrogène qui ont une réelle spécificité, les liaisons multiples qui offre un déterminisme assez performant et les liaisons simples qui montrent les limites de ce déterminisme, par leur complexité et leur superposition aux autres modes de vibrations.
Les élongations associant l'hydrogène.
Après un bref rappel sur l'oscillateur harmonique, ce thème sera composé de 3 parties relatives aux types d'élongation \(\textrm{X-H}\) :
élongation \(\textrm{C-H}\),
élongation \(\textrm{O-H}\),
élongation \(\textrm{N-H}\).
Rappel :
Rappelons que le modèle de l'oscillateur harmonique permet de déterminer, de manière théorique et approximative, la "fréquence" de l'absorption correspondant à la vibration d'une liaison entre deux atomes. C'est le nombre d'onde associé à la vibration de la liaison :
\(\mathrm{\bar \nu = \frac{1}{2.\pi.c}\sqrt{\frac{k}{\mu}}}\)
avec
k constante de force de la liaison
\(\mu\) masse réduite des deux atomes
c vitesse de la lumière
Le nombre d'onde s'exprime en \(\mathrm{cm}^{-1}\).
Ainsi, le nombre d'onde associé à la vibration de la liaison dépend à la fois
de la masse des deux atomes liés (par la masse réduite \(\mu\))
de la nature de la liaison entre ces deux atomes (par la constante de force \(\textrm k\)).
Il en résulte que les liaisons faisant intervenir un atome d'hydrogène ont des fréquences de vibration d'élongation nettement supérieures à toutes les fréquences de vibration d'élongation des autres liaisons. Ceci provient du fait que l'hydrogène a une masse inférieure à celle de tous les autres éléments intervenant dans les molécules organiques.
De manière globale, la variation de k est plus faible que celle de \(\mu\). La constante de force k ne varie au maximum que d'un facteur 3 (au maximum, les recouvrements \(\pi\) étant moins liants que la liaison \(\sigma\)) quand on passe de la liaison simple à la liaison triple. La variation relative de la masse réduite \(\mu\) est beaucoup plus importante.
D'autre part, il est intéressant de remarquer que la masse réduite \(\mu\) tend globalement vers la masse du plus petit atome de la liaison. Ainsi \(\mu\) tend vers la masse du carbone \(\textrm C\) pour toutes les liaisons impliquant l'atome de carbone. En effet :
\(\mu=\mathrm{\frac{m_1\times m_2}{m_1+m_2}=\frac{m_1\times m_2}{m_1\times \left(1+\frac{m_2}{m_1}\right)}=\frac{m_2}{1+\frac{m_2}{m_1}}}\)
Si \(\textrm m_1\), la masse la plus grande, croît, le rapport \(\textrm m_2 \textrm{/ m}_1\) tend vers 0 et la masse réduite tend vers la masse \(\textrm m_2\) du plus petit atome.
Liaisons | C-H | C-C | C-F | C-Cl | C-Br | C-I |
Masses réduites en \(\mathrm{\mu~en~10^{-26}~kg}\) | 0,15 | 0,99 | 1,21 | 1,48 | 1,73 | 1,82 |
Ne mémorisez pas ces chiffres | ||||||
La variation relative de la masse réduite m est beaucoup plus importante. Aussi, le facteur prépondérant pour la variation de la "fréquence" est la masse réduite \(\mu\), la constante de force \(\textrm k\) ayant une influence moindre.
Ainsi, les masses réduites \(\mu\) des liaisons impliquant l'hydrogène et un autre élément auront la masse de l'hydrogène comme limite inférieure, soit \(1,67. 10^{-27}\textrm{ kg}\). L'atome d'hydrogène étant le plus léger des éléments, les liaisons impliquant l'hydrogène ont donc des fréquences de vibration d'élongation nettement plus élevées que toutes les autres liaisons.
Les bandes d'absorption Infra Rouge de plus haute énergie correspondent donc aux vibrations d'élongation des liaisons avec l'hydrogène.
Pour les composés organiques, l'atome le plus léger après l'hydrogène, excepté le deutérium, est le carbone (on a, en effet, \(\textrm C : 12\), \(\textrm N : 14\), \(\textrm O : 16\)). De ce fait, les masses réduites \(\textrm m\) des liaisons impliquant le carbone et un autre élément autre que l'hydrogène ou le deutérium, auront la masse du carbone comme limite inférieure, soit \(19,9 .10^{-27}\textrm{ kg}\). Il faut noter que la partie des hautes fréquences correspondant aux liaisons avec de l'hydrogène sera nettement différenciée de la partie correspondant aux liaisons impliquant du carbone.
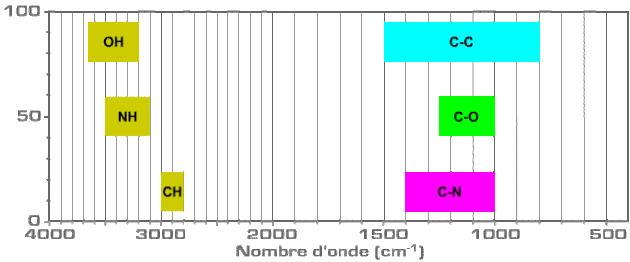
Observons les plages des vibrations des liaisons impliquant l'hydrogène \(\textrm{H-O}\),\(\textrm{ H-N}\) et \(\textrm{H-C}\) et les plages des vibrations des liaisons impliquant le carbone \(\textrm{C-C}\), \(\textrm{C-N}\) et \(\textrm{C-O}\) :
Il apparaît nettement que les plages de vibration des liaisons comportant de l'hydrogène diffèrent de celles des liaisons comportant du carbone.
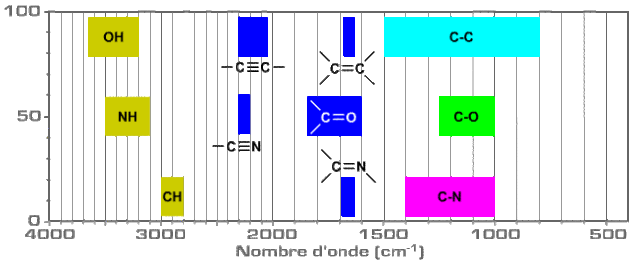
Observons maintenant l'influence de la nature de la liaison simple, double ou triple :
Le passage de la liaison simple, à la liaison double, à la liaison triple, entraîne un accroissement de la constante de force \(\textrm k\) avec l'ordre de la liaison et justifie une augmentation des valeurs des plages de fréquences observées.
La fréquence de vibration est fonction de la constante de force de la liaison \(\textrm k\) et de la masse réduite \(\mu\). Pour l'hydrogène qui ne peut former qu'une simple liaison, la variation de la constante de force est relativement faible. La variation de la masse réduite est également limitée par la faible valeur de la masse de l'hydrogène. Ces deux facteurs concourent à réduire le domaine de variation de la fréquence de vibration des liaisons impliquant l'hydrogène.