Élongations C-H
On distingue deux types de vibrations :
les vibrations d'élongation (mouvements relatifs des atomes suivant leur axe de liaison)
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
les vibrations de déformation (mouvements avec variation des angles de liaison).
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
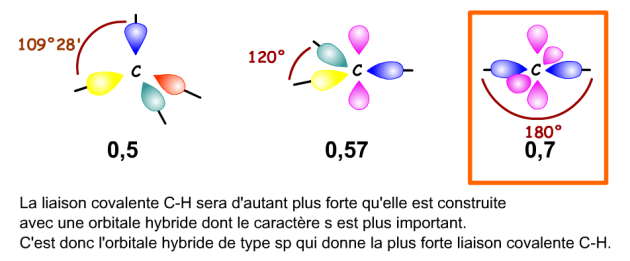
C'est la variation de la constante de force de la liaison \(\textrm{C-H}\) qui provoque la variation de la fréquence de la vibration d'élongation. Cette variation de la constante de force est liée à l'augmentation au caractère s de l'orbitale hybride du carbone qui participe la liaison
Rappel :
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
La constante de force, donc la fréquence de vibration d'élongation de la liaison \(\textrm{C-H}\) varie dans le même sens que le caractère s.
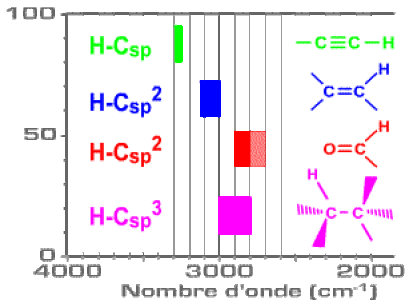
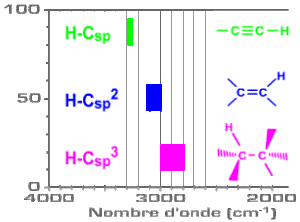
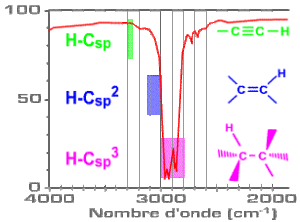
La fréquence de vibration d'élongation de la liaison C-H augmente donc quand on passe | de la simple liaison | à la double liaison | à la triple liaison |
| | | |
Ainsi, selon l'hybridation du carbone | \(\mathrm{sp^3}\) | \(\mathrm{sp^2}\) | \(\mathrm{sp}\) |
les fréquences d'absorption varient autour de | \(2950 ~\mathrm{cm^{-1}}\) | \(3050~ \mathrm{cm^{-1}}\) | \(3300~\mathrm{ cm^{-1}}\) |
Fondamental :
Retenez que c'est la variation de la constante de force de la liaison \(\textrm{C-H}\), due au changement du type d'hybridation du carbone, qui provoque la variation de la fréquence de la vibration d'élongation.
Sous haute résolution, il est possible d'analyser un peu plus en détail ces plages de fréquences. Considérons d'abord le cas des liaisons\( \textrm{H-C}\) \(\textrm{sp}^3\) ce qui correspond aux groupes \(\textrm{>CH-}\), \(\textrm{-CH}_2-\) et \(\textrm{-CH}_3\). Les \(\textrm{-CH}_2-\) et \(\textrm{-CH}_3\) donnent des élongations symétriques et asymétriques.
Vibration d'élongation symétrique dans le plan de la molécule.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Vibration d'élongation asymétrique dans le plan de la molécule.
Ces absorptions apparaissent vers :
\(2960~ \mathrm{cm^{-1}}\) asymétrique pour les \(-\textrm{CH}_3\)
\(2930 ~\mathrm{cm^{-1}}\) asymétrique pour les \(-\textrm{CH}_2-\)
\(2880~\mathrm{ cm^{-1}}\) symétrique pour les \(-\textrm{CH}_3\)
\(2860~\mathrm{ cm^{-1}}\) symétrique pour les \(-\textrm{CH}_2-\).
Par contre, le groupement \(>\textrm{CH}-\) ne donne qu'une absorption, d'intensité beaucoup plus faible, située vers \(2890~\mathrm{ cm^{-1}}\) .
Vous aurez en général des spectres enregistrés en basse résolution. Dans ce cas on observe l'enveloppe de ces différentes bandes avec parfois quelques épaulements comme vous le montre la partie \(4000-2000 ~\mathrm{cm^{-1}}\) du spectre Infra Rouge de l'heptane comportant 5 \(-\textrm{CH}_2-\) et 2 \(-\textrm{CH}_3\). On observe l'enveloppe de ces bandes d'élongation \(\textrm{C-H}\) car la molécule comporte plusieurs groupes méthylènes et méthyles différents.
Un groupe méthylène \(\textrm{-CH}_2-\) présente 2 élongations \(\textrm{C-H}\) : élongation symétrique et asymétrique.
Un groupe méthyle \(-\textrm{CH}_3\) présente 3 élongations \(\textrm{C-H}\) : une élongation symétrique et deux élongations asymétriques.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
En fait, ces 3 bandes sont généralement noyées avec celles des méthylènes et on observe une enveloppe. Rares sont les cas où l'on peut les distinguer.
Considérons maintenant le cas des liaisons \(\textrm{H-C}\) \(\textrm{sp}^2\) (\(\textrm H\) éthyléniques ou aromatiques) dont la fréquence de vibration d'élongation est comprise entre 3000 et \(3100~\mathrm{ cm^{-1}}\). Quand le carbone de la liaison \(\textrm{H-C}\) \(\textrm{sp}^2\) porte un oxygène (cas de l'aldéhyde \(\textrm{H-C=O}\)) on a une diminution sensible de la fréquence. Il faut noter que la présence d'un groupement électronégatif adjacent au \(\textrm{C-H}\) entraîne toujours une diminution sensible de la fréquence.
Pour un aldéhyde, on observera l'élongation \(\textrm{H-C=O}\) vers 2800-2700 \(\textrm{cm}^-1\) qui est très caractéristique car elle n'interfère pas avec d'autres plages.
Une deuxième bande vers 2900-2800 \(\textrm cm^-1\) correspond à une bande harmonique (en fait une résonance de Fermi). Cette bande est "noyée" dans les bandes d'élongation des \(\textrm{C-H}\) aliphatiques et n'est pas visible sauf dans certains cas (aldéhydes aromatiques par exemple).