Degrés de libertés.
Nous avons vu qu'une molécule diatomique peut être regardée comme un système de 2 masses reliées par une liaison ayant des propriétés voisines de celles d'un ressort. De la même manière, une molécule polyatomique, peut être regardée comme un système de plusieurs masses reliées entre elles par des liaisons ayant des propriétés voisines de celles de ressorts.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
On sait maintenant calculer de manière théorique, la fréquence d'absorption d'une vibration moléculaire. Il nous reste donc à savoir déterminer le nombre de vibrations possibles que peut posséder une molécule. La détermination du nombre de modes vibrationnels possibles pour une molécule devrait permettre de prévoir le nombre d'absorptions observables sur le spectre Infra Rouge de cette molécule. Nous allons nous intéresser dans un premier temps à la détermination du nombre de modes de vibration possibles d'une molécule.
Trois coordonnées sont nécessaires pour positionner un atome dans l'espace. De manière générale, on appelle degré de liberté chaque information nécessaire au positionnement d'une entité dans l'espace. Ainsi, on dira qu'un atome possède 3 degrés de liberté.
De manière générale, chaque atome possède 3 degrés de liberté. Les liaisons n'entraînent pas de modification du nombre de degrés de liberté. Pour une molécule constituée de n atomes, on aura \(3.\textrm n\) degrés de liberté. Donc pour une molécule diatomique, on aura 6 degrés de libertés
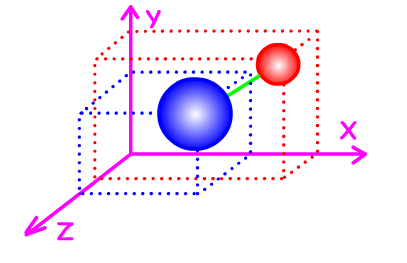
Pour une molécule constituée de \(\textrm n\) atomes, on aura \(3.\textrm n\) degrés de liberté.
Pour une molécule diatomique, on aura 6 degrés de libertés. Voici ces 6 degrés de liberté.Ces degrés de liberté se décomposent en différents modes.On distingue des modes de translation, de rotation et de vibration.
Le mode de translation correspond à un déplacement identique de chaque atome de la molécule.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Le mode de rotation correspond à une rotation de la molécule autour de son centre d'inertie.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Le mode de vibration correspond à un déplacement différent de chaque atome de la molécule, le centre d'inertie de la molécule restant fixe.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Visualisons plus en détails ces 6 types de liberté : soit une molécule diatomique placée dans un référentiel dont l'axe des X est parallèle à la liaison entre les deux atomes.
Translation :
Parallèlement à l'axe des Z :
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Parallèlement à l'axe des X :
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Parallèlement à l'axe des Y :
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Dans un espace à 3 dimensions, on a 3 types de translation. La translation décrite par le positionnement du centre d'inertie de la molécule n'implique que 3 degrés de liberté.
Rotation :
Parallèlement au plan Z,O,Y ;
il s'agit alors d'une rotation axiale le long de la liaison. La rotation autour de l'axe de liaison ne change en rien les coordonnées et donc n'implique aucun degré de liberté.
Parallèlement au plan X,O,Y :
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Parallèlement au plan Z,O,X :
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Vibration :
Vibration : elle se produit le long de la liaison.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Généralisation :
De manière générale, nous avons vu qu'une molécule quelconque constituée de n atomes possédait 3n degrés de liberté. Dans le cas d'une molécule possédant 3 atomes, nous aurons donc \(3 \times 3 = 9\) degrés de libertés.L'espace étant à 3 dimensions, toute molécule ne peut posséder que 3 modes de translation.Nous venons de voir que les molécules linéaires étant déjà positionnées sur un axe, ne possèdent que 2 modes de rotation. Par contre, les molécules non linéaires vont posséder 3 modes de rotation.
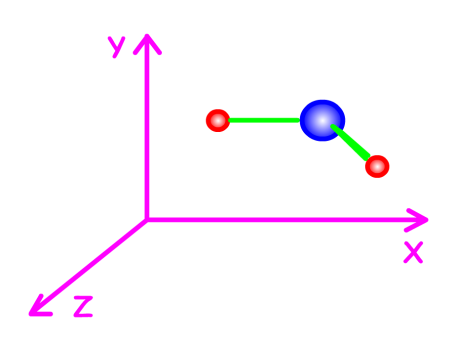
Rotation selon l'axe des X
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Rotation selon l'axe des Y
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Rotation selon l'axe des Z
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
En résumé
Modes de libertés de la molécule | linéaire exemple : \(\mathrm{CO_2}\) | non linéaire exemple : \(\mathrm{H_2O}\) |
degrés de libertés | 3n | 3n |
modes de translation | 3 | 3 |
modes de rotation | 2 | 3 |
modes de vibration | 3n-5 | 3n-6 |
La spectroscopie Infra-Rouge étant une technique analytique qui permet d'observer les vibrations moléculaires, on pourra donc déterminer ainsi facilement le nombre de modes de vibration. Ce nombre de modes de vibration correspond au nombre MAXIMUM de bandes que l'on devrait pouvoir observer dans le spectre Infra Rouge d'une molécule. En effet, tout mode de vibration n'est pas systématiquement observé.