Isochronie
Deux protons d'une molécule ne conduisent pas nécessairement à deux signaux !
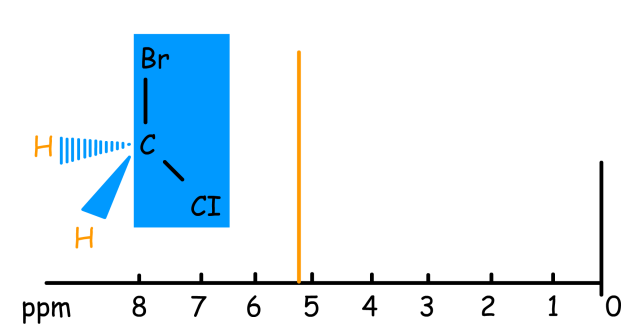
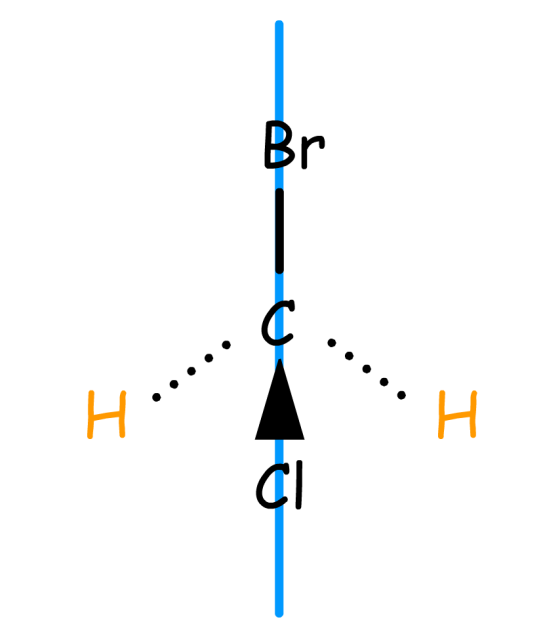
On observe, par exemple, un signal unique lorsque deux protons ont un environnement identique. Considérons la molécule de bromo-chlorométhane dont nous avons fait figurer les trois atomes \(\textrm{Cl}\), \(\textrm C\) et \(\textrm{Br}\) dans le plan représenté en bleu.
Ce plan est bissecteur de l'angle formé par les deux atomes d'hydrogène et le carbone.
Il en résulte que les deux atomes d'hydrogènes perçoivent un environnement identique, et que la résonance de chacun est atteinte pour le même champ ; on dit qu'il y a isochronisme.
Exemple :
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Mis à part le signal du TMS que l'on ne considérera plus... on peut observer ici un seul signal pour 3 protons... Pourquoi ?
Une situation d'isochronisme où 3 atomes d'hydrogène perçoivent un même environnement se retrouve dans le cas de tout groupement METHYLE.
Vous pouvez le voir sur ce spectre du cyanure de méthyle. Dans cette molécule, du fait de l'existence d'un axe de symétrie d'ordre 3, chacun des atomes perçoit de façon identique chacun des trois autres atomes.
Les 3 \(\textrm H\) sont donc identiques.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Dans le cas du chlorure d'acétyle il n'existe aucun axe de symétrie. Mais, à température ambiante, il n'y a pas de conformation privilégiée qui différencie un hydrogène par rapport aux deux autres.
De par la libre rotation \(\textrm{C-C}\), chaque proton subit statistiquement un environnement moyen identique.
Cela se traduit encore par un signal unique pour les trois atomes d'hydrogène du groupement méthyle.
Remarque :
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
L'isochronisme n'est pas limité au cas des protons portés par un seul atome, on le retrouve chaque fois que des protons se trouvent dans un environnement identique.
Ainsi, dans la pyrazine, dont les traces des éléments de symétrie figurent en pointillés, les quatre Carbone \(sp_2\) (de forme trigonale) portent chacun un atome d'hydrogène qui perçoit un environnement similaire à celui perçu par les trois autres. De ce fait, on observe un seul signal de résonance.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Les symétries et la libre rotation expliquent pourquoi l'on n'observe qu'un seul signal pour les 3 méthyles du bromure de tertio butyle.
Les neuf protons du tBu sont toujours isochrones.
Douze protons sont isochrones dans le cas du tétra méthyle silane... le composé de référence.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Dans un certain nombre d'espèces chimiques, on rencontre simultanément plusieurs situations d'isochronisme.
Tel est le cas, par exemple, pour l'hexaméthylbenzène de Dewar ou hexaméthyl [2,2,0]bicyclohexa-1,3-diène.
Dans ce composé, les deux méthyles en tête de pont perçoivent un environnement d'un premier type, distinct de celui des quatre autres méthyles.
Dans le cas du pinacol, c'est l'existence d'une libre rotation \(\textrm{C-C}\) qui entraîne statistiquement un environnement identique, d'une part pour les protons des quatre méthyles, d'autre part pour les protons des deux hydroxyles. On observe donc deux signaux.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Impossible d'accéder à la ressource audio ou vidéo à l'adresse :
La ressource n'est plus disponible ou vous n'êtes pas autorisé à y accéder. Veuillez vérifier votre accès puis recharger le média.
Dans le cas de la pipérazine, il faut savoir que celle-ci existe essentiellement sous forme chaise. Si nous considérons l'une des deux conformations par exemple celle qui est représentée, on doit s'attendre à observer trois signaux : d'une part celui des protons portés par l'azote et d'autre part, deux signaux caractéristiques, l'un des protons axiaux et l'autre des protons équatoriaux.
Comme vous pouvez le voir, on n'observe qu'un seul signal pour les protons portés par les carbones ! Voyons pourquoi.A température ambiante, on a équilibre entre deux conformations...
Considérons le conformère du bas. Le proton figuré en violet y occupe une position équatoriale. Dans l'autre conformère, obtenu par interconversion, ce même proton occupe alors une position axiale !
A température ambiante (condition habituelle de réalisation du spectre), l'interconversion entre les deux conformères est très rapide et le proton figuré en violet perçoit en définitive un environnement moyenné.
La situation est symétrique pour le proton figuré en vert et par extension pour tous les protons portés par un carbone de cette molécule. Finalement, un seul signal sera observé pour les protons axiaux et équatoriaux. La situation serait différente si on réalisait le spectre à basse température... mais c'est une autre histoire...