L'effet gamma
L'effet gamma est assez inattendu, de part son importance, puisqu'on observe un blindage moyen de l'ordre de -2,5 ppm qui peut atteindre -6 ppm et plus encore, alors que le substituant se trouve en position \(\gamma\) ce qui correspond au troisième carbone. Nous avons vu cette situation pour les alcanes pour le calcul des déplacements chimiques.
Dans le cas des alcanes non ramifiés, on devait rajouter des incréments \(\textrm A_j\) à la valeur de départ, celle correspondant au déplacement chimique du méthane, à savoir -2,3 ppm...
\(\alpha : + 9,1 \mathrm{ppm}\) | \(\beta : + 9,4 \mathrm{ppm}\) | \(\gamma : - 2,5 \mathrm{ppm}\) | \(\delta : + 0,3 \mathrm{ppm}\) | \(\epsilon : + 0,1 \mathrm{ppm}\) |
Ainsi pour le n-octane \(\textrm{CH}_3\textrm{-CH}_2\textrm{-CH}_2\textrm{-CH}_2\textrm{-CH}_2\textrm{-CH}_2\textrm{-CH}_2\textrm{-CH}_3\), on obtient :
Incréments | Valeur expérimentale observée | |
|---|---|---|
\(\mathrm{CH_3}\) | \(\delta=\mathrm{-2,3+A\alpha+A\beta+A\gamma+A\delta+A\epsilon}\) \(\delta=\mathrm{-2,3+9,1+ 9,4 - 2,5 + 0,3+0,1}\) \(\delta =\mathrm{14,1~ ppm}\) | 13,6 ppm |
\(\mathrm{CH_2}\) | \(\delta=\mathrm{-2,3+2A\alpha+A\beta+A\gamma+A\delta+A\epsilon}\) \(\delta=\mathrm{-2,3+(2\times9,1)+ 9,4 - 2,5 + 0,3+0,1}\) \(\delta =\mathrm{23,2~ ppm}\) | 22,7 ppm |
\(\mathrm{CH_2}\) | \(\delta=\mathrm{-2,3+2A\alpha+2A\beta+2A\gamma+A\delta}\) \(\delta=\mathrm{-2,3+(2\times9,1)+ (2\times9,4) - 2,5 + 0,3}\) \(\delta =\mathrm{32,6~ ppm}\) | 32,1 ppm |
\(\mathrm{CH_2}\) | \(\delta=\mathrm{-2,3+2A\alpha+2A\beta+2A\gamma+A\delta}\) \(\delta=\mathrm{-2,3+(2\times9,1)+ (2\times9,4) -2\times 2,5 + 0,3}\) \(\delta =\mathrm{30,0~ ppm}\) | 29,4 ppm |
En fait, ajouter un nouveau carbone (\(\textrm{CH}_3\) par exemple) en \(\gamma\) conduit à une chaîne de 4 carbones, et en considérant les hydrogènes portés par les deux carbones terminaux, nous obtenons une chaîne à 6 atomes consécutifs qui permet un rapprochement fort (de l'ordre de l'angstrom) entre deux des hydrogènes de chacun de ses carbones terminaux. C'est la figure, bien connue des organiciens, des cycles non tendus à 6 atomes alors que tout cycle moins important ne se ferme que sous de fortes tensions et laisse supposer une plus forte distance entre ces hydrogènes, et que pour des chaînes supérieures à 6 atomes, intervient un rapprochement excessif qui se traduira par une répulsion entre noyaux des atomes.
S'agissant de la RMN, les deux hydrogènes ainsi rapprochés voient leurs nuages électroniques déplacés vers leurs carbones porteurs du fait de la répulsion électrostatique ; il s'en suit un blindage du carbone. Un effet \(\gamma\) fort traduit à la fois une proximité importante et une durée de vie forte de cette conformation induisant la répulsion. Elle est donc plus forte dans le cas des cycles, et très bien décrite pour leur méthylation, notamment pour le cyclohexane.
Terme constant (relatif au TMS) : 27,3 ppm.
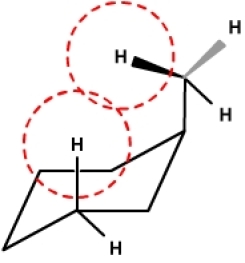
Pour le carbone situé en position \(\gamma\) du carbone porteur du méthyle \(\textrm{CH}_3\) en position équatoriale, on n'observe pas d'effet de compression et de ce fait l'incrément est de +0,05 alors que dans le cas de la substitution en position axiale, on observe une interaction entre les protons du \(\textrm{CH}_3\) et le proton en position axiale porté par le carbone \(\gamma\) ce qui explique la forte valeur blindante -6,37.