Orden de reacción
Definición :
En ciertos casos, la ley de velocidad puede expresarse de una forma simple de tipo:
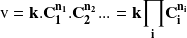
Decimos, entonces, que la reacción admite un orden.
Los exponentes
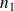 ,
,
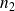 .. son constantes independientes de las concentraciones y del tiempo, y se llaman órdenes parciales.
.. son constantes independientes de las concentraciones y del tiempo, y se llaman órdenes parciales.
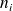 es del orden parcial de la reacción con respecto al componente
es del orden parcial de la reacción con respecto al componente
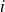 .
.
La suma de los órdenes parciales
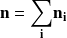 es el orden global de la reacción. Si no hay ambigüedad, decimos, simplemente, orden de la reacción.
es el orden global de la reacción. Si no hay ambigüedad, decimos, simplemente, orden de la reacción.
Los valores más corrientes de los órdenes parciales son 1 y 2.
También encontramos valores fraccionarios (
 ,
,
 ,
,
 ) o negativos (-1) o incluso, reales.
) o negativos (-1) o incluso, reales.
Cuando la velocidad no depende de la concentración de un reactante, decimos que la reacción es de orden cero con respecto a dicho reactante.






