Cycloalcanes
Pour les cycloalcanes en dehors d'effet de contrainte importante les \(\textrm{CH}_2\) des cycles saturés oscillent entre 25 et 29.7 ppm (\(\textrm{CH}_2\) centraux des chaînes longues ouvertes) pour des cycles non substitués. Les substitutions alkyles vont introduire des effets voisins de ceux observés pour les chaînes ouvertes, déblindants en \(\alpha\) et \(\beta\), blindant en \(\gamma\). Mais avec les cycles apparaissent des conformations plus ou moins stables, loin de la libre rotation qui caractérise les chaînes ouvertes. Dans ces conditions les effets sont non seulement dépendants de l'éloignement ( \(\alpha\), \(\beta\), \(\gamma\),..), mais de la position sur le cycle. Cette situation est très nette sur le cyclohexane dont les positions axiale et équatoriale sont bien connues.
Le tableau ci-dessus montre les effets de l'ajout d'un groupe méthyle \(\textrm{CH}_3\) sur les déplacements chimiques des carbones du cyclohexane (dont les carbones résonnent à 27,3 ppm quand il n'est pas substitué). On observe des incréments qui diffèrent fortement selon que le \(\textrm{CH}_3\) est axial ou équatorial.
On retrouve assez bien l'effet \(\beta\) nettement déblindant, l'effet \(\alpha\) déblindant (mais moins fort) et surtout un effet \(\gamma\) très prononcé quand le méthyle est en position axiale.
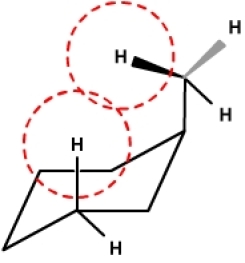
Pour le carbone situé en position du carbone porteur du méthyle \(\textrm{CH}_3\) en position équatoriale, on n'observe pas d'effet de compression et de ce fait l'incrément est de +0,05 alors que dans le cas de la substitution en position axiale, on observe une interaction entre les protons du \(\textrm{CH}_3\) et le proton en position axiale porté par le carbone \(\gamma\) ce qui explique la forte valeur blindante -6,37.